Hyalexo CROSS
Notre dispositif médical à base de hyaluronate de sodium à 3% réticulé pour injection intra-articulaire
Dosage 90 mg / 3 ml
Boite de 1 seringue pré-remplie
Mono-injection d’acide hyaluronique réticulée
Notre dispositif médical à base de hyaluronate de sodium à 3% réticulé pour injection intra-articulaire
Dosage 90 mg / 3 ml
Boite de 1 seringue pré-remplie
Mono-injection d’acide hyaluronique réticulée
Hyalexo CROSS

Hyalexo CROSS
Acide hyaluronique réticulé
CONSEILS D'UTILISATION
HYALEXO CROSS 3%/90mg/3mL
DESCRIPTION
HYALEXO CROSS se présente sous forme d'un gel visqueux, transparent, viscoélastique et incolore. Il contient un gel à base d'acide hyaluronique réticulé, d'un volume de 3 mL, dans une seringue stérile et apyrogène. Comme le produit possède des propriétés viscoélastiques et présente une capacité de liaison élevée aux molécules d'eau, il agit comme lubrifiant, normalise la viscosité du liquide synovial et est utilisé sous forme d'un gel stérile qui soutient le tissu conjonctif intra-articulaire. Le produit contient de l'acide hyaluronique réticulé obtenu par fermentation bactérienne, à une concentration de 30 mg/mL, et dissous dans une solution saline physiologiquement tamponnée. La totalité du gel correspond à de l'acide hyaluronique réticulé obtenu par fermentation avec un tampon phosphate.
INDICATIONS
HYALEXO CROSS est indiqué dans les troubles articulaires douloureux provoqués par des maladies dégénératives ou post-traumatiques ou des lésions articulaires. Grâce aux propriétés viscoélastiques du gel, le produit aide les articulations à maintenir leur état rhéologique et physiologique optimal. Il contribue à améliorer la fonction articulaire et à réduire les symptômes douloureux. Il est indiqué pour le traitement de la douleur chez les patients souffrant d'arthrose du genou. Les effets du produit sont liés à la lubrification et l'amélioration mécanique.
UTILISATION PRÉVUE
HYALEXO CROSS doit être utilisé uniquement par des médecins qualifiés (orthopédie-traumatologie, rhumatologie, médecine physique et de réadaptation, spécialistes en médecine du sport ou équivalents) et formés à la technique de l'injection intra-articulaire.
CONTRE-INDICATIONS
• Ne pas utiliser ce produit chez des patients présentant une hypersensibilité aux préparations à base d'acide hyaluronique.
• Ne pas administrer aux personnes présentant une hypersensibilité (allergie) connue aux protéines des bactéries gram-positives.
• Ne pas injecter dans l'articulation du genou chez des patients présentant des infections ou des maladies de peau au niveau du site d'injection ou de l'articulation.
• Ne pas administrer si le site d'injection prévu est le siège d'une douleur, d'une infection ou de signes d'une maladie aiguë ou chronique.
• Ne pas injecter chez les patients présentant des troubles hémorragiques systémiques connus.
MISES EN GARDE
• Éviter d'utiliser des désinfectants contenant des sels d'ammonium quaternaire pour la préparation de la peau en même temps que le produit.
• Lorsque des sels d’ammonium quaternaire - comme le chlorure de benzalkonium - sont mélangés à des solutions d’acide hyaluronique, ils peuvent former un précipité.
• Ne pas injecter par voie intravasculaire car cela pourrait entraîner des événements indésirables systémiques.
PRÉCAUTIONS D’EMPLOI
• Lors de l'administration, une technique stricte d'injection aseptique doit être utilisée.
• Le produit doit être injecté exclusivement dans l'articulation du genou affectée, par un médecin qualifié ou un professionnel de santé maîtrisant les procédures d'injection intra-articulaire, et dans des locaux adaptés à de telles injections.
• Ne pas injecter dans les vaisseaux sanguins, en dehors de l’articulation, ni dans les tissus synoviaux ou la capsule articulaire.
• Si la pression d’injection augmente, cela peut indiquer un positionnement extra-articulaire incorrect de l’aiguille ou l'injection d'une quantité excessive de gel dans l’articulation.
• Le patient doit être soigneusement examiné avant l'administration afin de détecter des signes d'inflammation aiguë et le médecin doit évaluer si un traitement doit être instauré dans ce cas.
• Retirer l'épanchement articulaire, le cas échéant, avant l'injection.
• En cas d'épanchement accompagné de douleurs intenses, le liquide doit préalablement être éliminé de l'articulation touchée.
• Des réactions locales transitoires peuvent survenir après une injection intra-articulaire, telles qu'une rougeur, un gonflement, par exemple. L'application locale de glace pendant 5 à 10 minutes peut réduire ces effets.
• La sécurité et l'efficacité de l'utilisation concomitante de HYALEXO CROSS avec d'autres produits injectables par voie intra-articulaire n'ont pas été établies.
• Ne pas utiliser si l'emballage est ouvert ou endommagé.
• Ne pas utiliser après la date de péremption indiquée sur l’emballage.
• Le produit ne doit pas être restérilisé car les performances du dispositif pourraient être compromises.
• Le produit n'a pas été testé sur des femmes enceintes ou des enfants de moins de 18 ans.
• Son innocuité et son efficacité n'ont pas été établies chez les femmes qui allaitent.
EFFETS INDÉSIRABLES
Effets indésirables rapportés dans la littérature après une injection intra-articulaire :
• Après des injections intra-articulaires, les patients peuvent ressentir une douleur et/ou un gonflement et/ou un épanchement articulaire temporaires. Dans certains cas d'infiltrations, des phénomènes d'inflammation aiguë de l'articulation traitée par injection intra-articulaire ont été rapportés, caractérisés par des douleurs articulaires, un gonflement, un épanchement et parfois avec chaleur et/ou raideur, rougeur, arthralgie.
• Les effets indésirables rapportés incluent des réponses à type d'hypersensibilité telles que des réactions anaphylactoïdes, un choc anaphylactique et un œdème de Quincke.
• Parfois, des cas légers à modérés de gonflement et d’inconfort temporaires ont été observés suite à l’injection intra-articulaire de préparations d’acide hyaluronique réticulé.
PRÉSENTATION
Chaque boîte contient 1 seringue préremplie contenant 3 mL de gel d'acide hyaluronique réticulé.
STÉRILISATION
Le produit est stérilisé à la vapeur. Le contenu de la seringue est stérile.
MODE D’ADMINISTRATION
Le produit doit être administré exclusivement par un professionnel de santé qualifié dans le cadre d'un traitement par injection intra-articulaire. Utiliser une aiguille de diamètre et de longueur adaptés en fonction de la localisation de l'articulation à traiter. Il est recommandé d'utiliser une aiguille à usage unique.
1. Une technique aseptique stricte doit être respectée lors de l’injection intra-articulaire.
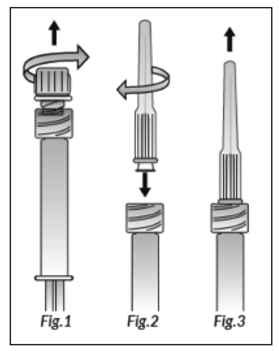
2. Retirez délicatement le capuchon protecteur de la seringue (Fig. 1).
3. Vissez fermement l'aiguille dans l'embout luer-lock (Fig. 2). Fixez fermement l'aiguille tout en maintenant fermement l'embout pour garantir une étanchéité parfaite et éviter les fuites pendant l'administration. Retirez-le protège-aiguille (Fig. 3). Ne pas trop serrer et ne pas appliquer de force excessive lors de l’insertion de l’aiguille ou du retrait du protège-aiguille, sinon l’embout de la seringue pourrait se briser.
4. Avant l'injection, le site d'injection doit être désinfecté avec un désinfectant approprié.
5. Le produit est ensuite injecté dans l'articulation.
CONSERVATION ET PÉREMPTION
Conserver le produit dans l'emballage d'origine, à une température comprise entre 2°C et 25°C, à l'abri de la lumière. NE PAS CONGELER.
La date de péremption est indiquée sur l'emballage.
FABRICANT
Semikal Teknoloji Sanayi ve Ticaret Anonim Sirketi
AOSB 3. Kısım Mah. 25. Cad. No:14/111 Dösemealtı, Antalya/TÜRKIYE
Tel: +90 246 237 01 01
www.semical.com.tr
DISTRIBUTEUR
Laboratoires Expanscience
1 place des Saisons
92048 Paris La Défense Cedex, France
Tel : 01 43 34 60 00
SYMBOLES PRÉSENTS SUR L'EMBALLAGE

Tout incident grave survenant en relation avec le dispositif médical doit être signalé au fabricant et à l’autorité compétente de l’État membre dans lequel l’utilisateur et/ou le patient est établi. Autorité compétente en France : Agence Nationale de Sécurité du Médicament et des produits de santé (ANSM) - Site internet : https://signalement.social-sante.gouv.fr/
HYX/NC.FR/24.04.2024/Rev00
top of page